Parmi les lois fondamentales qui régissent la thermodynamique, la loi zéro occupe une place cruciale, puisqu'elle établit les notions fondamentales de température et d'équilibre thermique.
La loi zéro de la thermodynamique stipule que « si deux systèmes sont en équilibre thermique avec un troisième système, ils sont également en équilibre entre eux ». Il est également connu sous le nom de principe zéro de la thermodynamique.
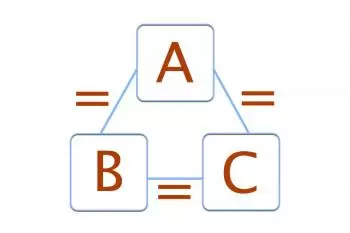
Si A est en équilibre avec B et A est également en équilibre thermique avec un troisième corps C, on peut conclure que B est en équilibre thermique avec C.
Deux corps sont en équilibre thermique lorsque, au contact, leurs variables d'état ne changent pas. S’ils ne sont pas en équilibre thermique, ils subiront un échange de chaleur ou d’énergie et atteindront l’équilibre thermique.
La loi zéro fut la dernière des lois de la thermodynamique à être introduite. Pour obtenir une structure logique, il fallait la placer avant les autres lois.
Formule de la 0ème loi de la thermodynamique
Principe 0 de la thermodynamique, si les trois systèmes sont en équilibre thermique, il faut compléter la formule suivante :
TA = TB = TC
Où TA , TB et TC sont les températures des trois systèmes.
Origine et histoire de la loi zéro
La loi zéro de la thermodynamique a été formulée pour répondre aux questions relatives à la mesure et à la comparaison des températures. Avant leur mise en place, les échelles de température étaient arbitraires et dépendaient de méthodes de mesure spécifiques. La nécessité de disposer d’une base plus solide pour comparer les températures était un sujet brûlant dans la communauté scientifique du XIXe siècle.
C'est le physicien allemand Gustav H. Johannsen qui a formulé pour la première fois l'idée centrale de la loi zéro dans les années 1860, mais ce n'est que dans les années 1930 qu'elle a été consolidée et incorporée comme loi fondamentale de la thermodynamique.
La loi zéro est ainsi appelée car elle constitue la base de la construction d’échelles de température et établit un principe fondamental pour mesurer la température.
Exemples de la loi zéro
Pour comprendre comment fonctionne la loi zéro de la thermodynamique, nous proposons trois exemples :
Glace et eau
On met un morceau de glace et un verre plein d'eau à température ambiante. Dans cette expérience trois éléments apparaissent : la glace, l'eau et le verre.
Dans un premier temps, les trois échangeront de la chaleur et de l’énergie jusqu’à atteindre l’équilibre thermique. Au bout d'un moment, les trois éléments atteindront la même température
Tasses de café
Imaginons deux tasses de café, une chaude et une froide. Lorsqu’elles entrent en contact, la chaleur circule de la tasse chaude vers la tasse froide jusqu’à ce que les deux atteignent la même température et soient en équilibre thermique.
Il s’agit d’un exemple pratique du principe zéro en action : les deux systèmes sont en équilibre thermique lorsqu’il n’y a plus de transfert net de chaleur entre eux.
Exemple de thermomètre
Un autre exemple qui permettra de mieux comprendre la notion d’équilibre thermique est celui d’un thermomètre.
Considérons un corps B constitué d'un tube avec un capillaire contenant du mercure. Leurs niveaux de hauteur au-dessus du capillaire représentent différentes températures.
Considérons maintenant un corps A, par exemple le corps humain. Si vous rapprochez le thermomètre de votre corps et le laissez suffisamment longtemps, le thermomètre atteindra la valeur correspondant à votre température corporelle.
Le thermomètre et le corps humain seront en équilibre thermique l’un avec l’autre. Les deux éléments atteignent donc la même température.